SEU Atipica e Terapia
Il trattamento della forma Atipica di Sindrome Emolitico Uremica (aSEU)
La SEU è una malattia rara e, come tale, poco conosciuta dai medici che non siano specialisti di essa. Questo focus sul trattamento della SEUa vuole aiutare pazienti e medici ad utilizzare opportunamente le risorse oggi disponibili.
Ciò che abbiamo scritto di seguito è frutto del contatto diretto con persone affette, dell’analisi attenta delle loro storie cliniche e dell’esito di esse.
Il materiale qui presentato non ha i caratteri di un articolo scientifico e non intende neppure averli, ma riteniamo che possa essere di fondamentale importanza per le persone affette da SEUa o che la contrarranno in futuro.
La SEU è una malattia grave ma oggi, a differenza di pochi anni orsono, ci sono gli strumenti per curarla bene purché vengano usati in modo tempestivo ed appropriato.
Speriamo che queste nostre riflessioni aiutino il paziente a comprendere, e quindi a vigilare, affinché tutto venga fatto al meglio visto che la vita è un bene prezioso ed è una sola. Peccato perderla perché colpiti da malattia rara e quindi poco conosciuta!
La forma Atipica di SEU
La diagnosi differenziale: tSEU o aSEU?
La Terapia della fase acuta
La Terapia con Ravulizumab
Allungamento intervallo di trattamento con Eculizumab
È possibile sospendere la Terapia con Eculizumab o Ravulizumab?
Monitoraggio recidive con stick urine nel paziente che ha sospeso la terapia
Gravidanza nella aSEU
Vaccinazioni Prevenzione delle infezioni associate a terapie con inibitori del complemento
Interventi chirurgici - Raccomandazioni per chi è portatore di variante genetica o ha interrotto la terapia con Eculizumab o Ravulizumab
Trapianto renale nella aSEU
La forma Atipica di SEU
La SEUa si presenta con un quadro clinico di microangiopatia trombotica, caratterizzata da consumo delle piastrine, emolisi meccanica (rottura dei globuli rossi e quindi fuoriuscita dell'emoglobina) e danno renale acuto.
Per la sua diagnosi è essenziale escludere che l’evento sia riconducibile alla SEU da STEC (nota come SEU tipica) che tuttavia si preannuncia sempre con disturbi gastrointestinali (diarrea). Purtroppo, se l'assenza di diarrea può escludere la SEUt da STEC, l'eventuale sua presenza non esclude con certezza che possa trattarsi di SEUa e quindi è quasi sempre necessaria un’indagine specifica di conferma che lo STEC sia presente (ricerca shigatossina nelle feci o ricerca anticorpi anti STEC) appunto perché occasionalmente anche la SEUa può essere associata a diarrea.
Andrà sempre ascritta alla SEU atipica ogni forma che:
-
- ricorra una seconda o più volte;
- si associ a familiarità (non coincidente nel tempo, come si può realizzare nelle epidemie familiari da STEC);
- se decorre con significativo consumo dei fattori del complemento (C3).
Un'altra malattia che può essere confusa con la SEUa, e che quindi andrà sempre esclusa, è la Porpora Trombotica Trombocitopenica (PTT) ove però un dosaggio dell'ADAMTS13 sarà diagnostico.
Così definita la SEUa include anche le forme da causa non nota e quelle che possono complicare altre patologie: infezioni pneumococciche, AIDS, trapianto di midollo, glomerulonefrite rapidamente progressiva, LES, tumori, acidemia metilmalonica e da farmaci o radioterapia.
La diagnosi differenziale: tSEU o aSEU?
Di fronte ad un caso di sospetta SEU è necessario circostanziare la diagnosi. Per questo è essenziale avviare subito le seguenti indagini:
se presente diarrea sarà indispensabile ricercare la shigatossina nelle feci (non il battere Escherichia Coli più comunemente ricercato nella maggioranza degli ospedali italiani) L’indagine dovrà essere fatta presto nel decorso della diarrea altrimenti si corre il rischio che la tossina non sia più presente, incorrendo in false negatività.
« Dove è possibile fare la ricerca del gene della Shigatossina 1 e 2 ? »
A nostra conoscenza, l’esame è effettuabile, al momento, presso:
Bari: Laboratorio di Epidemiologia Molecolare dell’U.O.C. Igiene dell’Azienda Ospedaliero Universitaria Consorziale Policlinico di Bari (Prof.ssa Maria Chironna) Telefono 080.5592328 - mail:
Milano: Centro per la cura e lo studio della SEU "Ilaria Destro" c/o Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico di Milano, (Dr. G. Ardissino). Numero telefonico attivo 24 su 24. 388.3086500 - email:
Roma: Laboratorio Nazionale di Riferimento per Escherichia Coli c/o Dipartimento di sanità Pubblica Veterinaria e Sicurezza Alimentare dell'Istituto Superiore di Sanità. Effettua attività diagnostica solo su richiesta di strutture del SSN e Università. Tel. 06.49902563 – 2727 email:
Se non è presente diarrea: sarà indispensabile il dosaggio dell'ADAMTS13 per escludere la PTT (particolarmente se l’interessamento renale è solo modesto) e avviare le indagini specifiche per la SEUa (genetica e ricerca anticorpi anti CFH).
« Dove è possibile condurre le Indagini Genetiche? »
A nostra conoscenza, l’esame è effettuabile, in tempi abbastanza rapidi, presso:
Centro per la cura e lo studio della SEU "Ilaria Destro" c/o Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico di Milano, (Dr. L.Porcaro, Dr. G. Ardissino) 02.55032432/3 – email:
Ci risulta che altri due centri italiani siano in condizione di condurre le indagini genetiche, ma considerati i tempi troppo lunghi di esecuzione degli stessi (4/6 mesi e oltre), che non sono congrui con le nostre aspettative, non riteniamo utile menzionarli.
Nell'attesa del risultato delle indagini specifiche un livello di C3 inferiore ai limiti di norma può essere altamente indicativo di una SEUa e quindi sufficiente per decidere di iniziare il trattamento con Eculizumab o Ravulizumab.
Una volta che la malattia è stata bloccata, ed i valori si sono stabilizzati, si potrà optare per diverse scelte terapeutiche: l’allungamento della distanza tra somministrazione o la sospensione del farmaco.
La Terapia della fase acuta
Sulla base della nostra esperienza (ovvero dell'esperienza di molti pazienti) siamo convinti che:
- Eculizumab o Ravulizumab è estremamente efficace per curare la SEUa. Molto più efficace della terapia tradizionalmente utilizzata: la plasmaferesi che è una terapia obsoleta e altamente inefficace.
- Se usato molto precocemente può cambiare radicalmente la prognosi della malattia.
- Quand'anche usato tardivamente (settimane o mesi dalla diagnosi) ha una discreta probabilità di spegnere la malattia e di fornire benefici che possono consentire alla persona di continuare a vivere una vita più normale. Molte persone, considerate ormai in insufficienza renale terminale, sono riuscite a recuperare una funzione renale che ha consentito loro di vivere per anni senza dialisi.
- Se usato in seconda battuta, dopo cicli di plasmaterapia, può residuare un’insufficienza renale, più o meno importante, che potrà richiedere la dialisi in un tempo successivo.
- La vaccinazione contro la meningite è utile ma non è essenziale per iniziare il trattamento con Eculizumab o Ravulizumab, può essere temporaneamente ovviata dalla profilassi con antibiotici.
- L’infusione del farmaco per via endovenosa va fatta, indipendentemente dal dosaggio, in circa 45 minuti.
Eculizumab o Ravulizumab deve quindi essere la terapia usata in prima linea (la plasmaterapia rappresenta il passato ed ha tassi di successo molto bassi) e deve essere usato presto nel corso della malattia.
La terapia con Ravulizumab
Il Ravulizumab è un farmaco in distribuzione solo da alcuni mesi e il suo utilizzo per il trattamento della SEU Atipica. Anche per le persone affette l’esperienza è diversa: alcune hanno già fatto più di una dose, ad altre non è ancora stato proposto.
Abbiamo ritenuto utile creare quindi una sezione dedicata a questo farmaco per aiutare le persone a conoscerlo meglio.
RAVULIZUMAB - DOMANDE E RISPOSTE
E’ importante innanzitutto che la persona affetta riceva adeguata informazione da parte del medico sulla procedura di passaggio al Ravulizumab, sul dosaggio e sugli intervalli di somministrazione. Il momento del confronto medico-paziente è un passaggio importantissimo in cui la persona affetta deve sentirsi libera di porre tutte le domande che ritiene utili e di sottoporre i propri dubbi. Chiedete di avere un incontro con il vostro medico di riferimento prima di iniziare la terapia e assicuratevi che vi venga dedicato il giusto tempo per assimilare le informazioni.
Le indicazioni fornite dal medico soprattutto in materia di prevenzione delle infezioni e di copertura vaccinale vanno seguite scrupolosamente.
Nel momento dell’infusione occorre sempre accertarsi che i tempi e le dosi di somministrazione corrispondano a quelli concordati con il medico e siano coerenti con quanto prescritto dal foglietto illustrativo, sotto qui descritte.
Tabella 1: Regime posologico di ravulizumab in base al peso corporeo per pazienti adulti affetti da SEUa con peso corporeo superiore o pari a 40 kg
| Intervallo di peso corporeo (kg) | Dose di carico (mg) | Dose di mantenimento (mg)* |
Intervallo di |
| da ≥ 40 a < 60 | 2400 | 3000 | Ogni 8 settimane |
| da ≥ 60 a < 100 | 2700 | 3300 | Ogni 8 settimane |
| ≥ 100 | 3000 | 3600 | Ogni 8 settimane |
* La prima dose di mantenimento è somministrata 2 settimane dopo la dose di carico.
Tabella 3: Regime posologico di ravulizumab in base al peso corporeo per pazienti pediatrici affetti da SEUa di peso inferiore a 40 kg
| Intervallo di peso corporeo (kg) | Dose di carico (mg) | Dose di mantenimento (mg)* | Intervallo di somministrazione |
| da ≥ 10 a < 20 | 600 | 600 | Ogni 4 settimane |
| da ≥ 20 a < 30 | 900 | 2100 | Ogni 8 settimane |
| da ≥ 30 a < 40 | 1200 | 2700 | Ogni 8 settimane |
* La prima dose di mantenimento è somministrata 2 settimane dopo la dose di carico.
Tabella 6: Velocità di somministrazione della dose di Ultomiris 300 mg/3 mL e 1100 mg/11 mL concentrato per soluzione per infusione
| Intervallo di peso corporeo (kg)a | Dose di carico (mg) | Durata minima dell'infusione minuti (ore) | Dose di mantenimento (mg) | Durata minima dell'infusione minuti (ore) |
| da ≥ 10 a < 20b | 600 | 45 (0,8) | 600 | 45 (0,8) |
| da ≥ 20 a < 30b | 900 | 35 (0,6) | 2100 | 75 (1,3) |
| da ≥ 30 a < 40b | 1200 | 31 (0,5) | 2700 | 65 (1,1) |
| da ≥ 40 a < 60 | 2400 | 45 (0,8) | 3000 | 55 (0,9) |
| da ≥ 60 a < 100 | 2700 | 35 (0,6) | 3300 | 40 (0,7) |
| ≥ 100 | 3000 | 25 (0,4) | 3600 | 30 (0,5) |
a Peso corporeo al momento del trattamento.
b Solo per le indicazioni EPN e SEUa.
Segnalare sempre all’infermiere o al medico eventuali sensazioni di malessere.
NOTA BENE
Al termine dell’infusione accertarsi che venga effettuato il lavaggio con almeno 20 ml di fisiologica o che tutto il liquido contenuto nel deflussore venga fatto scendere e quindi infuso per gravità.
Questo passaggio è molto importante perché il Ravulizumab è un farmaco molto concentrato (ogni flacone da 300 mg è costituito da solo 3 ml), e viene diluito con una proporzione di 1 a 1.
I deflussori delle normali pompe infusionali possono contenere dai 6 ai 18 ml di liquido; quando la pompa si blocca perché la sacca di infusione è vuota, nel deflussore possono rimanere quindi dai 6 ai 18 ml di farmaco, cioè dai 300 ai 900 mg.
Per una persona di peso compreso tra i 40 e i 60 kg ciò significherebbe assumere fino al 30% in meno della dose di sua competenza.
Fai presente al medico o all’infermiere questo dettaglio che potrebbe fare la differenza per la tua salute.
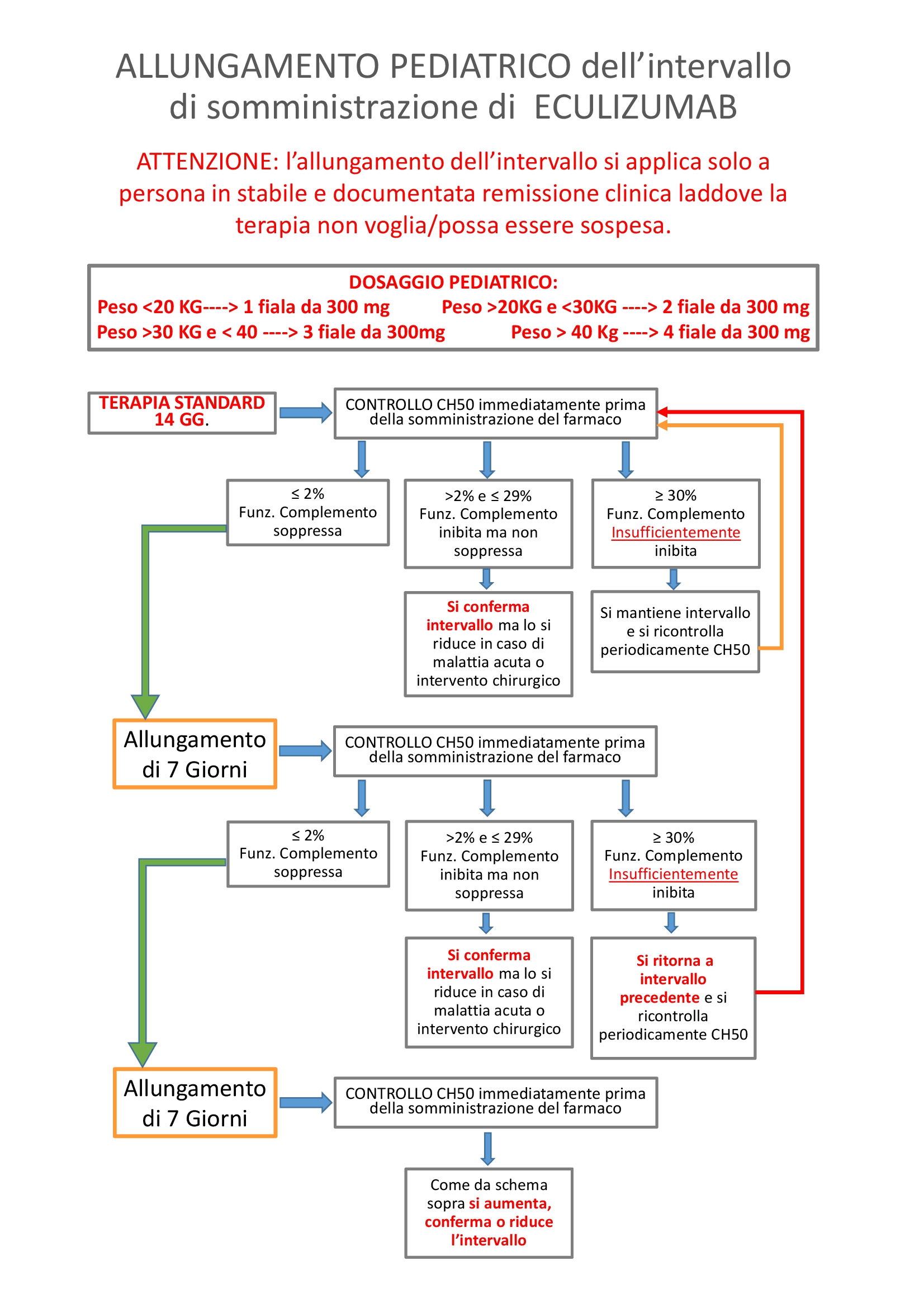
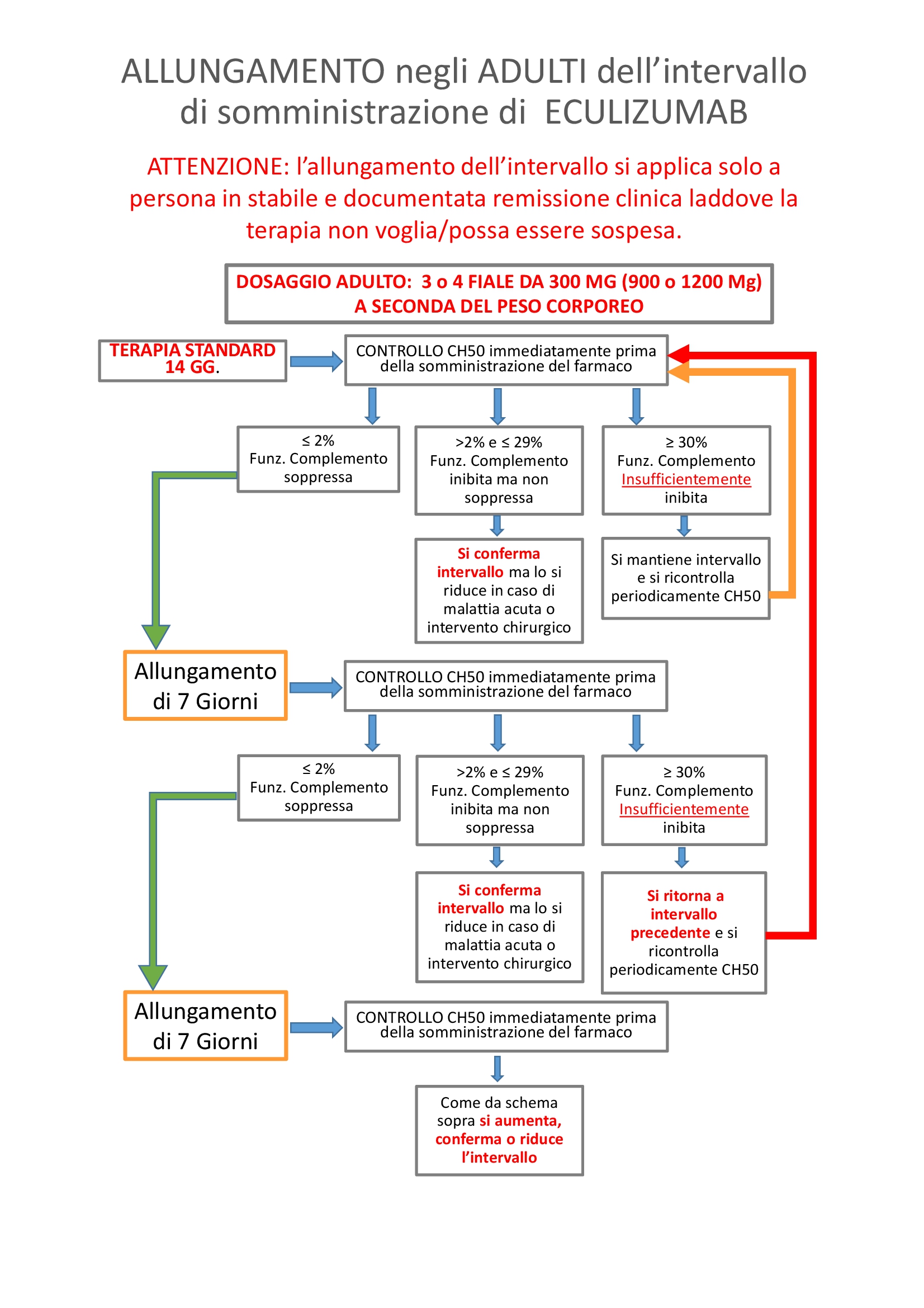
Allungamento intervallo di trattamento con Eculizumab
La prosecuzione del trattamento è elemento meno critico del suo inizio perché, una volta ottenuta la remissione della fase acuta, c'è tempo per decidere, anche sulla base delle indagini specifiche quale sia la migliore scelta.
Tra le opzioni disponibili vi è la sospensione della terapia o la sua individualizzazione sulla base della funzione globale del complemento (allungamento della distanza tra somministrazioni).
È bene sapere che esiste una modalità di somministrazione diversa da quella standard (ogni 2 settimane).
Il farmaco inibisce il sistema del complemento, nella quasi totalità dei pazienti, per un periodo più lungo di due settimane ed il monitoraggio della funzione globale del complemento, attraverso il monitoraggio dei livelli di CH50 e/o AP50 consente di individualizzare la cadenza delle somministrazioni sulle effettive necessità (efficacia biologica) e non a cadenza fissa.
Alcuni ospedali utilizzano il livello di C5b-9 come indicatore di efficacia del farmaco, ma purtroppo, l’esperienza ha dimostrato che questo parametro non è sufficientemente attendibile per il monitoraggio dell’efficacia del trattamento.
L’allungamento tra somministrazioni a 21 o 28 giorni, consente al paziente un miglioramento della qualità di vita a parità di risultato terapeutico, ci si deve recare meno volte in ospedale per la terapia (ogni 3 settimane 17 volte, ogni 4 settimane 13 volte, anziché 26 volte l’anno), si minimizza il rischio di meningite (notoriamente presente in coloro che abbiano un deficit a carico della catena del complemento), riduce ulteriormente la probabilità di sensibilizzazione al farmaco (quest’ultimo al momento solo teorico poiché il farmaco è stato sempre ben tollerato ma che va a crescere con la continuativa esposizione) modulando la dose in funzione delle dimensioni del paziente (molte volte è sufficiente un dosaggio di 900 mg).
Nel contempo si realizza un importante risparmio che può andare dal 33% al 50% e più. Questo ovviamente consentirà di fornire la cura a più persone rendendo il trattamento stesso competitivo rispetto al costo della dialisi.
Ad oggi, molte persone sono sottoposte a terapia individualizzata, mantenendo comunque la malattia in stato di remissione.
NOTE DA LEGGERE ATTENTAMENTE
I dati scientifici raccolti evidenziano che l’intervallo di somministrazione della terapia è difficilmente aumentabile oltre i 35 giorni.
Sulla base dell’esperienza del Centro per la Cura e lo Studio della SEU della Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico di Milano, meno del 5% dei pazienti rimane a 14 gg, il 30% rimane a 21 gg, il 60% rimane a 28 gg e il 5% va a 35 gg.
Bibliografia: “Ardissino G, Tel F, Sgarbanti M, Cresseri D, Giussani A, Griffini S, Grovetto E, Possenti I, Perrone M, Testa S, Paglialonga F, Messa P, Cugno M (2017) Complement functional tests for monitoring eculizumab treatment in patients with atypical hemolytic uremic syndrome: an update. Pediatr Nephrol. 10.1007/s00467-017-3813-2”
Ogni aumento dell’intervallo di somministrazione deve essere effettuato misurando i livelli di CH50, in modo da ridurre al minimo le possibilità di RECIDIVA di Sindrome Emolitico Uremica.
Se ciò non viene fatto, la PERSONA NON DEVE ACCETTARE l’allungamento dell’intervallo di somministrazione.
A tutela delle parti, l’allungamento della terapia deve essere praticato attraverso la stesura di un consenso informato sottoscritto dalla persona affetta da SEU e dal medico che indichi con precisione le modalità ed i controlli che verranno effettuati.
BENEFICI per le PERSONE dell’aumento dell’intervallo della terapia:
- recarsi meno volte in ospedale con conseguente minor tempo sottratto al lavoro o alla scuola, al tempo libero ed alla vita familiare con minor costi per gli spostamenti da e verso il centro di cura;
- minore esposizione al farmaco;
- sentirsi psicologicamente meno legati all’ospedale e quindi meno malati;
- preservare maggiormente i vasi sanguigni.
La persona ha quindi nel complesso una migliore qualità di vita.
In ultimo, l’aumento dell’intervallo porta ad un significativo risparmio della spesa sanitaria che può essere messo a disposizione della collettività e di altre persone che dovranno intraprendere percorsi di cura.
COME EFFETTUARE L'ALLUNGAMENTO DELLA TERAPIA
È possibile sospendere la terapia con Eculizumab o Ravulizumab?
In alcuni pazienti stabilmente in remissione e con buona funzione renale residua è possibile prevedere anche la sospensione della terapia di mantenimento. Questo vale soprattutto per le forme che non presentino mutazioni genetiche specifiche, per i soggetti con anticorpi anti CFH (qualora il titolo si sia ridotto) ed i deficit di MCP e CFI.
È possibile che la malattia recidivi, ma se il paziente è adeguatamente monitorato (stick urine per monitorare la microematuria 2-3 volte/settimana e quando non sta bene), la recidiva viene prontamente intercettata ed il trattamento viene immediatamente ripreso. La presenza di microematuria allo stick urine dovrà sempre indurre un approfondimento con gli esami del sangue alla ricerca dei segni tipici della microangiopatia trombotica.
La recidiva così gestita, in diversi casi ha comportato solo un fugace e temporaneo peggioramento della funzione renale con una normalizzazione della stessa nel giro di pochi giorni.
Alla luce delle attuali conoscenze, non appare saggio interrompere il mantenimento nei soggetti sottoposti a tx renale, particolarmente se da mutazione a carico del CFH (in quanto la recidiva potrebbe pregiudicare in modo definitivo l’organo trapiantato anche attraverso l’innesco di un rigetto), in coloro che presentano una funzione renale già gravemente compromessa (sCr> 2.5 mg/dL), in tutti coloro che hanno già presentato recidiva a breve dopo un primo tentativo di sospensione.
Monitoraggio recidive con stick urine nel paziente che ha sospeso Eculizumab
Nelle persone affette da SEU Atipica che abbiano interrotto il trattamento con Eculizumab o con Ravulizumab il primo segno di recidiva di malattia è la comparsa di microematuria (sangue nelle urine). Allo scopo di effettuare una diagnosi precoce delle recidive e di riprendere tempestivamente la terapia, è quindi di fondamentale importanza il monitoraggio domiciliare periodico attraverso lo stick urine che suggeriamo di effettuare regolarmente attraverso il seguente schema di massima:
| PERIODO DI SOSPENSIONE | FREQUENZA STICK URINE |
| Tra 14 gg e 2 Mesi | 3 VOLTE A SETTIMANA |
| Tra 2 e 6 Mesi | 2 VOLTE A SETTIMANA |
| Tra 6 e 12 Mesi | 1 VOLTE A SETTIMANA |
| Dopo i 12 Mesi | IN OGNI OCCASIONE DI MALATTIA (PER ESEMPIO INFEZIONE RESPIRATORIA, GASTROINTESTINALE, INTERVENTI CHIRURGICI, TRAUMI) O QUANDO LA PERSONA SI SENTA POCO BENE, ALMENO 2 VOLTE A SETTIMANA |
- Raccogliere un campione di urine (evitando di utilizzare la prima minzione del mattino).
- Immergere la striscia reattiva nelle urine e rimuoverla immediatamente.
- Lasciar la striscia reattiva in posizione orizzontale per 60 secondi.
- Confrontare la colorazione della striscia a livello dell’Hb (‘BLOOD’) con la scala colorimetrica posta sulla confezione degli stick.
- In caso di positività lieve (+) si raccomanda di ripetere il test dopo 12 ore;
- dopo 12 ore se positività maggiore (≥++) si raccomanda di avvertire immediatamente il medico curante per l’approfondimento sul sangue;
- In caso di dubbia/lieve positività ripetere ogni 12 ore fino a negativizzazione e/o positivizzazione franca (≥++). Nel caso di positivizzazione avvertire il medico curante.

Gravidanza nella aSEU
È noto che la gravidanza ed il parto rappresentano importanti fattori scatenanti la aSEU con gravi rischi di vita per il feto e per la mamma. L’Eculizumab è stato efficacemente utilizzato in gravidanza senza effetti collaterali sia per curare la aSEU che per prevenzione della recidiva di malattia.
Vaccinazioni Prevenzioni delle infezioni associate a terapie con inibitori del complemento
Il meningococco (Neisseria meningitidis) è un batterio molto diffuso caratterizzato da 13 sierotipi diversi; solo i sierotipi A, B, C, W135 e Y sono frequente causa di malattia meningococcica.
L’infezione si trasmette attraverso la respirazione. Questo batterio è presente normalmente nel naso e nella gola di molte persone senza provocare malattia.
Le infezioni da meningococco iniziano di solito in modo improvviso, con i seguenti sintomi:
- Febbre
- Mal di testa intenso;
- Rigidità del collo o della schiena;
- Stato confusionale;
- Dolori muscolari intensi associati a sintomi simil-influenzali;
- Fastidio alla luce.
Le persone in terapia con Eculizumab o Ravulizumab o analoghi inibitori del complemento sono esposti ad un maggior rischio di contrarre infezioni, particolarmente da Meningococco, Pneumococco ed Haemophilus Influenzae.
Per tale motivo, oltre a vigilare con attenzione sui segni e sintomi di tali infezioni (in particolar modo la febbre senza sintomatologia specifica associata), è indispensabile che la persona sia sottoposta alle vaccinazioni e relativi richiami per le malattie più pericolose e/o più frequenti.
Di seguito forniamo le raccomandazioni alla luce delle attuali conoscenze:
MENINGOCOCCO
- Vaccino coniugato tetravalente (MenACWY):
- 2 dosi a distanza di 8-12 settimane con richiamo ogni 3 anni (se il primo ciclo è stato effettuato a < 7 anni);
- ogni 5 anni (se il primo ciclo è stato effettuata a ≥ 7 anni).
- Vaccino per Meningococco B:
- per i bambini di età <2 aa un ciclo primario con 2 dosi distanziate di almeno 2 mesi. Richiamo dopo 1 anno dal termine del ciclo primario e successivamente ogni 3 anni;
- Per bambini > 2 anni e adulti: un ciclo primario con 2 dosi distanziate di almeno 1 mese. Richiamo dopo 1 anno dal termine del ciclo primario e successivamente ogni 3 anni.
PNEUMOCOCCO
- Vaccino coniugato 13-valente (PCV13):
- una dose nei bambini che non abbiano mai ricevuto il vaccino anti pneumococco.
HAEMOPHILUS INFLUENZAE
- Persone <12 mesi secondo calendario vaccinale;
- Persone 1-5 aa:
- non vaccinate (o che abbiano ricevuto solo 1 dose prima dei 12 mesi di vita): 2 dosi a distanza di 8 settimane;
-
chi abbia ricevuto 2 dosi prima dei 12 mesi di vita: 1 dose a 8 settimane dall’ultima dose (ovvero dalla seconda) e comunque il prima possibile;
-
chi abbia completato il ciclo primario e abbia ricevuto una dose di richiamo all’età ≥ 12 mesi: nessuna dose aggiuntiva.
- Persone di età >5 aa o adulti se mai immunizzati: 1 sola dose.
Bibliografia:
- Mbaeyi SA, Bozio CH, Duffy J, Rubin LG, Hariri S, Stephens DS, MacNeil JR. Meningococcal Vaccination: Recommendations of the Advisory Committee on Immunization Practices, United States, 2020. MMWR Recomm Rep. 2020 Sep 25;69(9):1-41. doi: 10.15585/mmwr.rr6909a1. PMID: 33417592; PMCID: PMC7527029.
- Meningococcal disease and the complement system. Lewis LA, Ram S. Virulence. 2014 Jan 1; 5(1):98-126. doi:10.4161/viru.26515. Epub2013Oct 8.
- Infections of People with Complement Deficiencies and Patients Who Have Undergone splenectomy. Ram S1, Lewis LA, Rice PA. Clin Microbiol Rev. 2010 Oct;23(4):740-80. doi: 10.1128/CMR.00048-09
- Matanock A, Lee G, Gierke R, Kobayashi M, Leidner A, Pilishvili T. Use of 13-Valent Pneumococcal Conjugate Vaccine and 23-Valent Pneumococcal Polysaccharide Vaccine Among Adults Aged ≥65 Years: Updated Recommendations of the Advisory Committee on Immunization Practices. MMWR Morb Mortal Wkly Rep 2019;68:1069–1075.
- Centers for Disease Control and Prevention (CDC). Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine among children aged 6-18 years with immunocompromising conditions: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Morb Mortal Wkly Rep. 2013 Jun 28;62(25):521-4. PMID: 23803961; PMCID: PMC4604951.
- Briere EC, Rubin L, Moro PL, Cohn A, Clark T, Messonnier N; Division of Bacterial Diseases, National Center for Immunization and Respiratory Diseases, CDC. Prevention and control of haemophilus influenzae type b disease: recommendations of the advisory committee on immunization practices (ACIP). MMWR Recomm Rep. 2014 Feb 28;63(RR-01):1-14. PMID: 24572654.
Le più comuni reazioni alla vaccinazione consistono in dolore, rossore, gonfiore e indurimento nel punto di iniezione che durano 1 o 2 giorni e si presentano nel 5-10% dei casi. Possono essere presenti febbre di intensità moderata, sonnolenza, cefalea e senso di malessere generale nel 2-5% dei casi. Raramente sono state osservate reazioni più severe come linfadenite, orticaria, reazioni anafilattoidi.
Interventi chirurgici - Raccomandazioni per chi è portatore di variante genetica o ha sospeso la terapia con Eculizumab o Ravulizumab
Le persone portatrici di varianti genetiche potenzialmente causative della SEU atipica e che non hanno mai manifestato la malattia, in occasione di malattie acute, interventi chirurgici o parto, dovranno mettere in atto un monitoraggio secondo queste indicazioni:
- Stick urine per emoglobinuria 3 giorni dopo l'evento da ripetersi per massima cautela 1 settimana dopo. Nel caso di emoglobinuria sarà indispensabile approfondire con tutto il pannello di accertamenti previsti per diagnosticare la microangiopatia trombotica: piastrine, emoglobina, LDH, aptoglobina, Creatinina + proteinuria/creatininuria ed esame urine completo.
- Nel caso in cui la patologia, la tipologia d’intervento, le procedure (catetere vescicale) prevedessero la presenza di ematuria, la precoce diagnosi di SEU dovrà per forza passare attraverso gli esami ematici sopra citati con i seguenti intervalli. Il giorno dopo l’intervento e a distanza di una settimana.
- Per le persone che in passato hanno avuto un episodio di aSEU e hanno interrotto la terapia con Eculizumab o Ravulizumab, va valutata con il proprio nefrologo una dose profilattica di farmaco prima dell’intervento.
Trapianto renale nella aSEU
Oggi, con l’uso di Eculizumab o Ravulizumab il trapianto renale, nei soggetti che in passato sono entrati in dialisi, ha ottime probabilità di successo.
Riteniamo importante che, in tutti i casi in cui sia stata posta una diagnosi di aSEU, sia stato identificato il deficit genetico o meno, venga somministrato il farmaco, prima di entrare in sala operatoria.
Riteniamo troppo rischioso non somministrare il farmaco ed iniziare il trattamento solo a fronte di una recidiva di SEUa.
Suggeriamo pertanto a tutti i candidati al trapianto per aSEU di farsi spiegare la procedura che verrà adottata alla chiamata per il trapianto e di vigilare perché essa contenga anche la somministrazione di Eculizumab o Ravulizumab pre trapianto (preventiva).
Su questa base e particolarmente per i deficit genetici più gravi (CFH), consigliamo ai pazienti di cambiare centro trapianti laddove non sia garantita la profilassi della recidiva mediante la procedura sopraindicata.
Sconsigliamo invece di aderire ad eventuale proposta di trapianto Rene-Fegato a causa degli elevati rischi per la vita con questa tipologia di trattamento, che oggi in Italia, in quasi tutti i casi, non rappresenta più una valida alternativa, per maggiori informazioni vi invitiamo a contattarci.
N.B.: Quando si effettua un trapianto, da cadavere o da donatore vivente, alcune cellule renali vengono inevitabilmente perse durante le fasi di prelievo, trasporto e trapianto; questo fà si che l’organo, benchè consenta una buona funzionalità, abbia ridotto rispetto a prima, la sua capacità di funzionamento; è chiaro che in caso di recidiva di SEU, esso subirebbe un ulteriore deterioramento che potrebbe diminuire la durata e la funzionalità dell’organo trapiantato, pertanto, considerate le possibilità terapeutiche disponibili, ci sembra importante riuscire ad evitare tutto ciò che sia evitabile.
Aggiungiamo inoltre che nel trapianto viene sostituito un solo rene, a maggior ragione se esso venisse danneggiato, il ritorno in dialisi sarebbe un passo breve.
A fronte di queste considerazioni, riteniamo sbagliato, troppo rischioso e incoerente con il passato (dove si predicava la non trapiantabilità), non somministrare il farmaco in via preventiva, ma attendere la recidiva di malattia.
In qualità di Associazione di pazienti, non vediamo in una simile scelta, alcuna motivazione scientifica, ma solo esigenze meramente economiche!
Problematiche relative al trattamento della aSEU
Il costo del trattamento
Il costo del trattamento con Eculizumab o Ravulizumab è ingente esso è, peraltro, interamente coperto dal Servizio Sanitario Nazionale. Nella nostra esperienza, l’elevato costo ha comportato una certa resistenza di alcuni medici all’impiego dell’Eculizumab o Ravulizumab (per questione di rispetto dei budget di spesa farmaceutica del reparto/ospedale). Questo comporta che in alcuni casi si preferisca, in prima battuta, seguire ancora la vecchia strada terapeutica della plasmaterapia che comunque ha un costo, sia in termini economici che in termini di disagio fisico per la persona affetta (accesso vascolare e sue complicanze) ma soprattutto ha un’efficacia di gran lunga inferiore se confrontata con quella dell’Eculizumab o Ravulizumab.
Riguardo a questo ci chiediamo: Una persona in dialisi non ha dei costi sanitari e sociali uguali o forse maggiori?
Riflessioni conclusive
- La terapia con Eculizumab o Ravulizumab deve essere iniziata senza indugio ed il suo inizio non deve essere subordinato al fallimento della plasmaferesi;
- La plasmaferesi ha un’efficacia decisamente inferiore rispetto all’Eculizumab o Ravulizumab;
- La gravidanza non rappresenta una controindicazione al trattamento con Eculizumab;
- Il trattamento può essere interrotto con appropriato monitoraggio, che consiste nell’esecuzione regolare (almeno 2 volte alla settimana) dello stick urine per la presenza di emoglobinuria. Lo stick urine andrà anche effettuato ogni volta che vi siano disturbi anche aspecifici;
- Il trattamento non deve essere interrotto nei portatori di trapianto renale ed in chi presenti una documentata frequente recidività della malattia;
- Chi debba proseguire il trattamento indefinitivamente potrà beneficiare di una posologia individualizzata sulla base della funzione globale del complemento (AP50 o CH50) che devono sempre rimanere a livelli più bassi rispetto al limite inferiore di norma.